Bienvenidos a la segunda clase virtual de Física II.
En esta sesión, abordaremos los siguientes Aprendizajes Esperados:
Aprendizaje esperado 10. Interpretar el calor como una forma de transferencia de energía.
Aprendizaje esperado 11. Distinguir entre los conceptos de calor, temperatura y energía interna.
Ahora bien, antes de reproducir el video y de leer el material didáctico proporcionado , te recuerdo que es tu deber como alumno notificar tu asistencia escribiendo en los comentarios, tu nombre completo empezando por los apellidos, así como tu grupo.
Si ya cumpliste con el pase de lista, te pido leas el material didáctico y que visualices el siguiente video proporcionado.
Introducción.
Cuando una sustancia se está fundiendo o evaporándose está absorbiendo cierta cantidad de calor llamada calor latente de fusión o calor latente de evaporación , según el caso . El calor latente, cualquiera que sea, se mantiene oculto, pero existe aunque no se manifieste un incremento en la temperatura, ya que mientras dure la fundición o la evaporación de la sustancia no se registrará variación de la misma.
Para entender estos conceptos se debe conocer muy bien la diferencia entre calor y temperatura .
En tanto el calor sensible es aquel que suministrado a una sustancia eleva su temperatura.

Calor: una forma de energía.
Q = m·Ce·(Tf-Ti)
La experiencia ha demostrado que la cantidad de calor tomada (o cedida) por un cuerpo es directamente proporcional a su masa y al aumento (o disminución) de temperatura que experimenta.
La expresión matemática de esta relación es la ecuación calorimétrica:
Bienvenidos a la segunda clase virtual de Física II.
En esta sesión, abordaremos los siguientes Aprendizajes Esperados:
Aprendizaje esperado 10. Interpretar el calor como una forma de transferencia de energía.
Aprendizaje esperado 11. Distinguir entre los conceptos de calor, temperatura y energía interna.
Ahora bien, antes de reproducir el video y de leer el material didáctico proporcionado , te recuerdo que es tu deber como alumno notificar tu asistencia escribiendo en los comentarios, tu nombre completo empezando por los apellidos, así como tu grupo.
Si ya cumpliste con el pase de lista, te pido leas el material didáctico y que visualices el siguiente video proporcionado.
Introducción.
Cuando una sustancia se está fundiendo o evaporándose está absorbiendo cierta cantidad de calor llamada calor latente de fusión o calor latente de evaporación , según el caso . El calor latente, cualquiera que sea, se mantiene oculto, pero existe aunque no se manifieste un incremento en la temperatura, ya que mientras dure la fundición o la evaporación de la sustancia no se registrará variación de la misma.
Para entender estos conceptos se debe conocer muy bien la diferencia entre calor y temperatura .
En tanto el calor sensible es aquel que suministrado a una sustancia eleva su temperatura.
 |
| Calor: una forma de energía. |
Q = m·Ce·(Tf-Ti)
La experiencia ha demostrado que la cantidad de calor tomada (o cedida) por un cuerpo es directamente proporcional a su masa y al aumento (o disminución) de temperatura que experimenta.
La expresión matemática de esta relación es la ecuación calorimétrica:
En palabras más simples, la cantidad de calor recibida o cedida por un cuerpo se calcula mediante esta fórmula, en la cual m es la masa, Ce es el calor específico, Ti es la temperatura inicial y Tf la temperatura final. Por lo tanto Tf – Ti = ΔT (variación de temperatura).
Nota: La temperatura inicial (Ti) se anota también como T 0 o como t 0 .
Si Ti > Tf el cuerpo cede calor Q < 0
Si Ti < Tf el cuerpo recibe calor Q > 0
Se define calor específico (Ce) como la cantidad de calor que hay que proporcionar a un gramo de sustancia para que eleve su temperatura en un grado centígrado. En el caso particular del agua Ce vale 1 cal/gº C ó 4,186 J.
En palabras más simples, la cantidad de calor recibida o cedida por un cuerpo se calcula mediante esta fórmula, en la cual m es la masa, Ce es el calor específico, Ti es la temperatura inicial y Tf la temperatura final. Por lo tanto Tf – Ti = ΔT (variación de temperatura).
Nota: La temperatura inicial (Ti) se anota también como T 0 o como t 0 .
Si Ti > Tf el cuerpo cede calor Q < 0
Si Ti < Tf el cuerpo recibe calor Q > 0
Se define calor específico (Ce) como la cantidad de calor que hay que proporcionar a un gramo de sustancia para que eleve su temperatura en un grado centígrado. En el caso particular del agua Ce vale 1 cal/gº C ó 4,186 J.
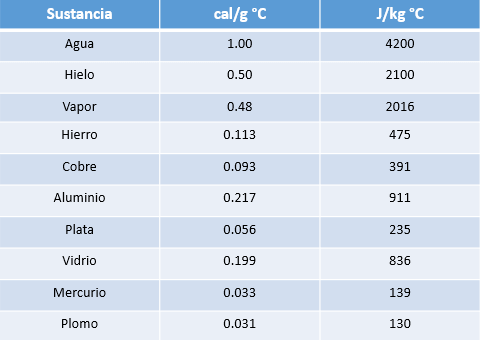
Tabla de Calores Específicos
De esta tabla, es posible concluir que la variación de temperatura de un cuerpo, al intercambiar cierta cantidad de energía térmica, depende del material de que está constituido dicho cuerpo (calor específico) y de su masa.
A continuación se presenta una tabla de calores específicos para realizar cálculo de cantidad de calor.
Para cumplir el objetivo de esta sesión se te solicita que revises el material didáctico el cual está disponible en la carpeta de la asignatura y posteriormente resuelve la actividad de aprendizaje correspondiente a esta segunda sesión y la enviarás ya resuelta a la dirección de correo electrónico gcaballero87@hotmail.com.
De esta tabla, es posible concluir que la variación de temperatura de un cuerpo, al intercambiar cierta cantidad de energía térmica, depende del material de que está constituido dicho cuerpo (calor específico) y de su masa.
A continuación se presenta una tabla de calores específicos para realizar cálculo de cantidad de calor.

Para cumplir el objetivo de esta sesión se te solicita que revises el material didáctico el cual está disponible en la carpeta de la asignatura y posteriormente resuelve la actividad de aprendizaje correspondiente a esta segunda sesión y la enviarás ya resuelta a la dirección de correo electrónico gcaballero87@hotmail.com.


Ruiz Hernandez Nayeli 2-B
ResponderEliminarPacheco González Luis angel 2-A
ResponderEliminarPacheco González Luis angel 2-A
ResponderEliminarSolis Cervantes Daymaru 2°E
ResponderEliminarPeniche Pérez Ariel Jose 2•E
ResponderEliminarEste comentario ha sido eliminado por el autor.
ResponderEliminarChale Amaro Erika 2°E
ResponderEliminarCalderón castillo Isaac Isai 2-A
ResponderEliminarNavarrete Euan América Guadalupe 2-E
ResponderEliminarRosado Tuz lesly Elizabeth 2E
ResponderEliminarChin Pacheco Alicia 2°B
ResponderEliminarCaballero Segura Geovanny Ricardo 2-B
ResponderEliminarlizama Villanueva paulina 2 Nocturno
ResponderEliminarMoreno Dzul Arleth Sarahí 2°"B"
ResponderEliminarAna Paola Arzapalo 2°A
ResponderEliminarOjeda Cancino Evelyn Aide 2A
ResponderEliminarPérez Magaña Joana Sinaí 2-A
ResponderEliminarRaúl García Méndez
ResponderEliminar2-A
tziu canche landy Lorena 2"A"
ResponderEliminarManuel Lizandro Aragon Cervantes 2-A
ResponderEliminarSantoyo Carrillo Fanny Alejandra, 2° "B"
ResponderEliminarMaría Goretti Torres Chab 2 A.
ResponderEliminarAguilar Ortiz Aldo Daniel 2C
ResponderEliminarRaúl Francisco Delgado Pat 2-A
ResponderEliminarCuellar guevara Ashley 2c
ResponderEliminarpacheco peña dilian monserrat 2C
ResponderEliminarLesli Dayan Canto Villanueva 2-A
ResponderEliminarJosé Antonio Canché Ramírez 2 C
ResponderEliminarRamírez Pérez Sergio de Jesús 2E
ResponderEliminarMoriel Cadeza Ana Laura 2D
ResponderEliminarCuellar guevara Ashley 2c
ResponderEliminarZubieta Gamboa Michelle 2A
ResponderEliminarChin Pacheco Alicia Cecilia 2°B
ResponderEliminarChin Pacheco Alicia Cecilia 2°B
ResponderEliminarshirley anai montejo cirerol 2 d
ResponderEliminarPlata Arjona Jennifer Alondra 2-D
ResponderEliminarRaigosa Fuentes Alejandra Sinaí 2-A
ResponderEliminarPompeyo Camargo Hendrik Fernando 2-B
ResponderEliminarDzul Villegas Miriam Cecilia 2A Nocturno
ResponderEliminarMoreno Dzul Arleth Sarahí 2°"B"
ResponderEliminarGutierrez Contreras Viviana Nicol 2C
ResponderEliminarochoa sierra rafael 2-E
ResponderEliminarCetina Castillo Yasuri Alejandra 2 A
ResponderEliminarPeña Cardenas Ginna Monserrat 2B
ResponderEliminarSanchez Nuñez Ariana Paulina 2:C
ResponderEliminarEstefany Beatriz Chable Canul 2D
ResponderEliminarChable Canul Estefany Beatriz 2D
ResponderEliminarsherly mishell ciau uicab 2A
ResponderEliminarMarrufo Miller Melissa 2°E
ResponderEliminarRuby Alejandra Novelo 2D
ResponderEliminarPolanco Romero yari rocio 2.A
ResponderEliminarRaúl García Méndez
ResponderEliminar2-A
Navarrete Euan América Guadalupe 2-E
ResponderEliminarCauich Briceño Mariany Isabel 2A
ResponderEliminarAzcorra Cauich Andry Gilberto "2-B"
ResponderEliminarEste comentario ha sido eliminado por el autor.
ResponderEliminarAvila Arjona Priscila del Rosario 2E
ResponderEliminarMoriel Cadeza Ana Laura 2D
ResponderEliminarColli Uc Karen Yazmin 2°B
ResponderEliminarSinai Monserrat Cardo Pech 2-D
ResponderEliminarChalé Balam Jairo Joel 2C
ResponderEliminarChan Cano Jesus Alberto 2.-B
ResponderEliminarRosado Tuz lesly Elizabeth 2E
ResponderEliminarClaudio Castañeda Alejandro 2E
ResponderEliminarhernandez bojorquez Sergio Oswaldo 2-B
ResponderEliminarGarcía Medina Yoal 2°B
ResponderEliminarAyala Borges Yaiza Guadalupe 2-B
ResponderEliminarDarling Esther Santos Gutierrez 2-A
ResponderEliminarAna Paola Arzapalo Chuc 2°A
ResponderEliminarKatya Jimena Ruiz Pool 2E
ResponderEliminarBaaz Ek Jessica Marian
ResponderEliminarWilliam Samuel Rivas nieves 2-A
ResponderEliminarcatzin pech izel esmeralda 2a noct
ResponderEliminarLeal Luna Axel Lael 2D
ResponderEliminarMoo Zozaya Julieta Guadalupe 2°C
ResponderEliminar